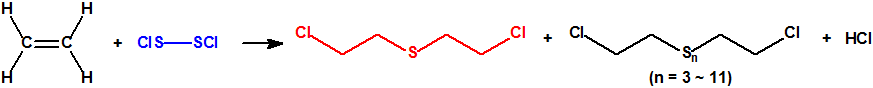
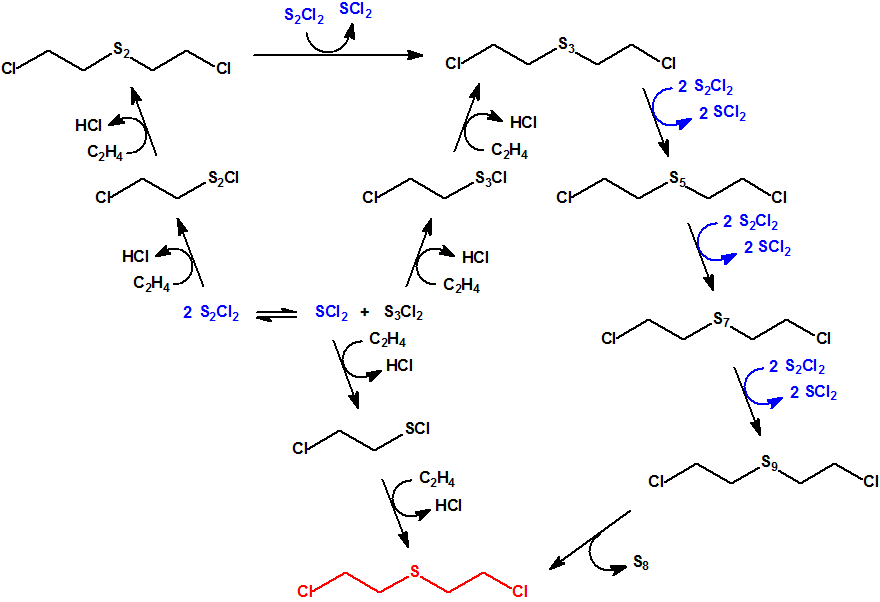
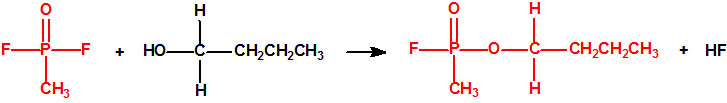El difluoruro de metilfosfonilo (DF), CAS 676-99-3, es un precursor de Lista 1 de la Convención sobre la prohibición de las Armas Químicas (CAQ) (1B.9), que está en la Lista de control de exportaciones del Grupo Australia, como precursor de armas químicas, junto con el dicloruro de metilfosfonilo (DC), CAS 676-97-1, precursor de Lista 2 de la CAQ (2B.4). Ambas sustancias se emplean como precursores en la síntesis de numerosos agentes neurotóxicos entre los que podemos citar el sarín (GB), el somán (GD) y el ciclosarín (GF).1
Muy probablemente, el DF era, antes de octubre del 2013, un completo desconocido para la inmensa mayoría de los lectores. A raíz del incidente con armas químicas en Ghouta (Siria) y de la adhesión de Siria a la CAQ en el año 2013, el DF se hizo muy popular y también la declaración inicial realizada por Siria sobre su arsenal químico.
Recordemos que las primeras noticias sobre el arsenal químico sirio hablaban de unas 1300 toneladas de iperita, sarín y VX, sin detallar más, pero con un texto ambiguo que daba a entender que las 1300 toneladas se referían a sustancias de lista 1A de la CAQ (agentes químicos de guerra). Lo cierto es que con los datos aparecidos el arsenal químico consistiría en 20,25 tm de iperita o gas mostaza (sustancia química tóxica de Lista 1A.4), 540 tm de DF o difluoruro de metilfosfonilo (precursor de Lista 1B.9), 290 tm de sustancias de Lista 2, 110 tm de sustancias de Lista 3, y 398 tm de sustancias químicas NO incluidas en el anexo de verificación de la CAQ, entre las cuales figuraban varios alcoholes (isopropanol, 1-butanol y metanol). Las cantidades de DF e iperita pueden variar ligeramente, en función de la fuente y la fecha de citación (570 tm de DF y 20,25 tmde iperita, 581 tm de DF y 19.8 tm de iperita, etc).2,3,4
El DF es un precursor llave, pues mezclado con diferentes alcoholes permite la obtención de manera muy sencilla de diversos agentes neurotóxicos, por ejemplo, sarín, somán y ciclosarín, todos ellos metilfosfonofluoridatos de O-alquilo. El DF es uno de los constituyentes del sistema binario de armas químicas más conocido, el GB2, para la obtención del sarín.
El DF5,6,7
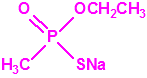
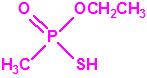
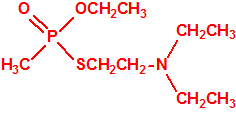
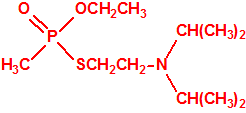
El difluoruro de metilfosfonilo (DF), tiene fórmula empírica CH3F2OP, estructura tetraédrica, y peso molecular 100,00:
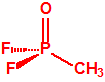
El difluoruro de metilfosfonilo (DF), también es conocido con otros nombres y sinónimos, como por ejemplo, difluoro, EA 1251, difluorometilfosfonato, óxido de difluorometilfosfina, metil difluorofosfito, ácido metilfosfonodifluorídico, etc.. El DF es una sustancia líquida de aspecto claro y olor acre, de punto de fusión -36,9 °C y punto de ebullición 99,7 °C, con una presión de vapor de 36 mmHg a 25 °C, la sustancia líquida es más densa que el agua (1,359 a 25 °C) y sus vapores son más densos que el aire (densidad relativa de los vapores = 3,4).
Los vapores de DF tienen un olor acre y pueden causar irritación dolorosa y severa de los ojos, nariz, garganta y pulmones. La exposición aguda severa puede causar edema pulmonar, cuya aparición podría retrasarse varias horas. En contacto con la piel el DF provoca una irritación severa de la misma, como consecuencia de la hidrólisis del DF por contacto con la humedad de la piel, con formación de fluoruro de hidrógeno, que podría causar quemaduras en la piel, de segundo o tercer grado. La ingestión del DF por via oral puede provocar una destrucción tisular severa en el tracto gastrointestinal.
Para una exposición laboral al DF, el valor límite sugerido para una jornada normal de trabajo de 8 horas y una semana laboral de 40 horas es de 0,008 mg/m3 (≅0,002 ppm). El valor establecido como Inmediatamente Peligroso para la Vida y la Salud, IPVS (Immediately Dangerous to Life or Health, IDLH) es de 0,01 ppm.
En caso de emergencia se recomienda emplear la guía de respuesta a emergencia nº 154 (GRE2016), correspondiente a sustancias tóxicas o/y corrosivas (no combustibles). El DF no es inflamable pero como reacciona con el agua para producir HF, en caso de incendio no se debería emplear agua, y debería emplearse CO2 o polvo.
Obtención8
- Los difluoruros de alquilfosfonilo pueden obtenerse a partir de los correspondientes dicloruros de alquilfosfonilo por reacción de éstos con fluoruro de hidrógeno anhidro, con excepción de los difluoruros de tert-butilfosfonilo que requieren un agente fluorante más potente, como por ejemplo, el trifluoruro de antimonio, y aún así, la reacción de fluoración puede no completarse, y quedarse en la formación del clorofluoruro de alquilfosfonilo:
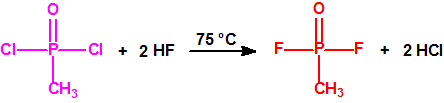
Normalmente, la reacción entre el fluoruro de hidrógeno y el dicloruro de metilfosfonilo es tan rápida que puede realizarse en el laboratorio con equipos de vidrio. La reacción con un mol de fluoruro de hidrógeno no conlleva a la formación del clorofluoruro de metilfosfonilo (CAS 753-71-9), sino más bien una mezcla de difluoruro de metilfosfonilo y dicloruro de metilfosfonilo que se pueden separarse por destilación.
Se funde el dicloruro de metilfosfonilo aumentando la temperatura hasta aproximadamente unos 35 °C y se añade fluoruro de hidrógeno anhidro a un ritmo tal que la temperatura se eleve hasta unos 75 °C. Durante la reacción se genera de manera ininterrumpida cloruro de hidrógeno. Si el sistema está perfectamente seco la reacción puede llevarse a cabo en vidrio Pyrex, con la línea de suministro de la bombona de fluoruro de hidrógeno hecha de polietileno, con un tubo de borboteo de cobre. El producto se desgasifica a presión reducida y el residuo se calienta a reflujo durante 30 minutos. El difluoruro de metilfosfonilo se separa mediante fraccionamiento con una pureza del 90%.
- También puede utilizarse como material de partida el ácido O-metil metilfosfónico en vez del dicloruro de metilfosfonilo:
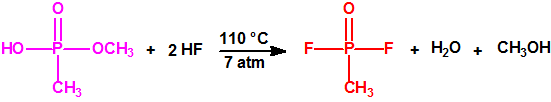
El ácido O-metil metilfosfónico (110 gramos ≅ 1 mol) y el fluoruro de hidrógeno anhidro (400 gramos ≅ 20 moles) se calientan a 110 °C y una presión de 7 atmósferas, durante 2 horas, en un autoclave de acero forrado de plata. La mezcla resultante se separa de la solución acuosa de fluoruro de hidrógeno y por destilación fraccionada se elimina el metanol. El rendimiento es del 60 %.
- Una ruta de síntesis diferente, hace reaccionar el metiltetrafluorofosforano (CAS 420-64-4) con el anhídrido acético (CAS 108-24-7) (puede utilizarse también anhídrido propiónico o anhídrido butírico):
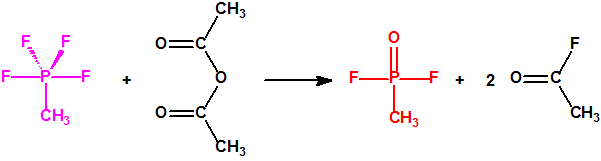
La reacción produce difluoruro de metilfosfonilo (DF) y fluoruro de acetilo (CAS 557-99-3) (con anhídrido propiónico o anhídrido butírico se formarían los correspondientes fluoruros de propionilo y de butirilo). El anhídrido del ácido se calienta a 80 °C y se hace pasar lentamente a través del metiltetrafluorofosforano. Para obtener el producto con buena pureza los productos se destilan dos veces.
Destrucción9
Para algunos agentes químicos de guerra existen los denominados sistemas binarios, donde los precursores (el denominado componente clave y un segundo componente) se encuentran en compartimentos separados por una membrana que se rompe con la inercia del disparo, de modo que los precursores se mezclan y reaccionan para formar el agente químico.
Para la destrucción de las armas químicas binarias la CAQ establece (en la Parte IV (A) – «Destrucción de armas químicas y su verificación de conformidad con el artículo IV», apartado «C. Destrucción», artículo 18) lo siguiente:
- A los efectos del orden de destrucción, se considerará que la cantidad declarada (en toneladas) del componente clave destinada a un producto final tóxico específico equivale a la cantidad (en toneladas) de ese producto final tóxico calculada sobre una base estequiométrica, suponiendo que el rendimiento sea del 100%;
- La exigencia de destruir una cantidad determinada del componente clave implicará la exigencia de destruir una cantidad correspondiente del otro componente, calculada a partir de la relación efectiva de peso de los componentes en el tipo pertinente de munición química binaria/dispositivo químico binario; y
- Si se declara una cantidad mayor de la necesaria del otro componente, sobre la base de la relación efectiva de peso entre componentes, el exceso consiguiente se destruirá a lo largo de los dos primeros años siguientes al comienzo de las operaciones de destrucción.
- Al final de cada año operacional siguiente, cada Estado Parte podrá conservar una cantidad del otro componente declarado determinada sobre la base de la relación efectiva de peso de los componentes en el tipo pertinente de munición química binaria/dispositivo químico binario.
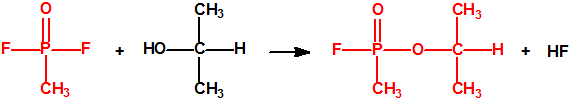
El apartado b. implica que no sólo se debe destruir todo el difluoruro de metilfosfonilo (DF) declarado, componente clave del sarín (Lista 1B), sino también la parte estequiométrica de alcohol isopropílico (sustancia no listada), por ser ambos componentes de un sistema binario del sarín. Es decir, por cada tonelada de DF se deben destruir 609 kilogramos de alcohol isopropílico.
 |
|
100,00 tm de DF + 60,90 tm de alcohol isopropílico producen 140,09 tm de sarín
Pero el DF es capaz de reaccionar con otros alcoholes para producir otros agentes neurotóxicos de la misma familia que el sarín (metilfosfonofluoridatos de O-alquilo, incluidos en la Lista 1A.1). |
 |
|
100,00 tm de DF + 102,17 tm de alcohol pinacolilico producen 82,17 tm de somán
|
 |
|
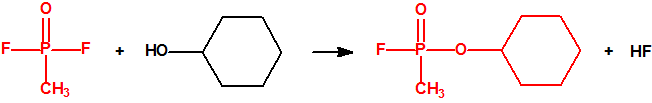
100,00 tm de DF + 100,16 tm de ciclohexanol producen 180,16 tm de ciclosarín
|
 |
|
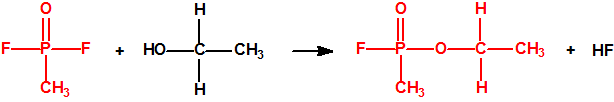
100,00 tm de DF + 46,07 tm de etanol producen 126,07 tm de metilfosfonofluoridato de O-etilo
|
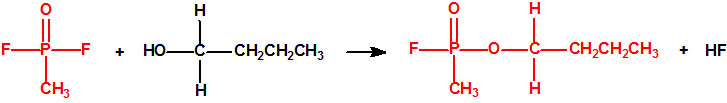 |
| 100,00 tm de DF + 74,12 tm de n-butanol producen 154,12 tm de metilfosfonofluoridato de O-butilo |
Habría que destruir el DF y en cada caso la correspondiente cantidad estequiométrica del alcohol en cuestión.
Hidrólisis5,7
El DF se hidroliza (reacciona con el agua) de manera prácticamente instantánea produciendo ácido metilfosfonofluorídico (MF, MethylphosphonoFluoridic acid, CAS 1511-67-7) y fluoruro de hidrógeno (HF), ambos tóxicos.
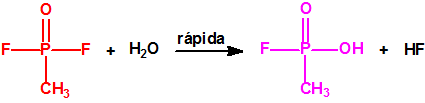
Como puede apreciarse, un mol de agua (18 gramos) reacciona con un mol de DF (100 gramos) para producir un mol de MF. El MF es una sustancia incluida en la Lista 2B.4 de la CAQ, y no sirve como precursor clave para la síntesis binaria del sarín (ni de ningún otro agente neurotóxico). La simple adición de agua al DF, así como la simple adición de agua al alcohol isopropílico, inutiliza ambos componentes para su utilización en la síntesis binaria del sarín.
La posterior hidrólisis del ácido metilfosfonofluorídico es una reacción lenta que produce ácido metilfosfónico (MPA, MethylPhosphonic Acid, CAS 993-13-5). Para el ácido metilfosfonofluorídico el tiempo de vida media, t½, es de 162 días a pH=7, de 90 días a pH=4 y de 47 días a pH=3.
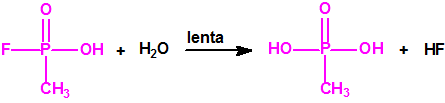
La reacción global sería:
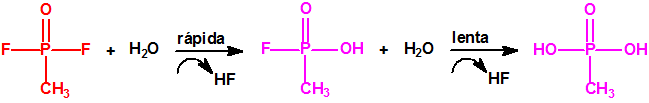
Según el Departamento de Defensa de Estados Unidos, a bordo de US Cape Ray se hidrolizaron 581,5 tm de DF y 19,8 tm de iperita utilizando dos unidades del sistema desplegable de hidrólisis (FDHS, Field Deployable Hidrolysis System)10 desarrollado por las Fuerzas Armadas de Estados Unidos (U.S. Army). El proceso duró 42 días y los efluentes resultantes de la hidrólisis y neutralización se entregaron en Finlandia y en Alemania, respectivamente, para su incineración.
El FDHS mezcla el DF con agua en una proporción 1:5. La hidrólisis produce principalmente una solución de ácido metilfosfonofluorídico (MPA, CAS 993-13-5) y ácido fluorhídrico (HF, CAS 7681-49-4). Esta solución de pH bastante ácido se transfiere a un contenedor de aleación hastelloy para su posterior neutralización hasta un pH ~7 empleando una solución de hidróxido sódico al 25 % (p/p). Como resultado de la neutralización el MPA se transforma en sus sales mono- y di-sódicas y el ácido fluorhídrico (HF) se transforma en fluoruro sódico (NaF, CAS 7681-49-4), todos ellos en solución acuosa5.

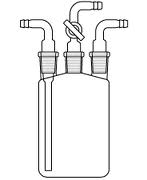
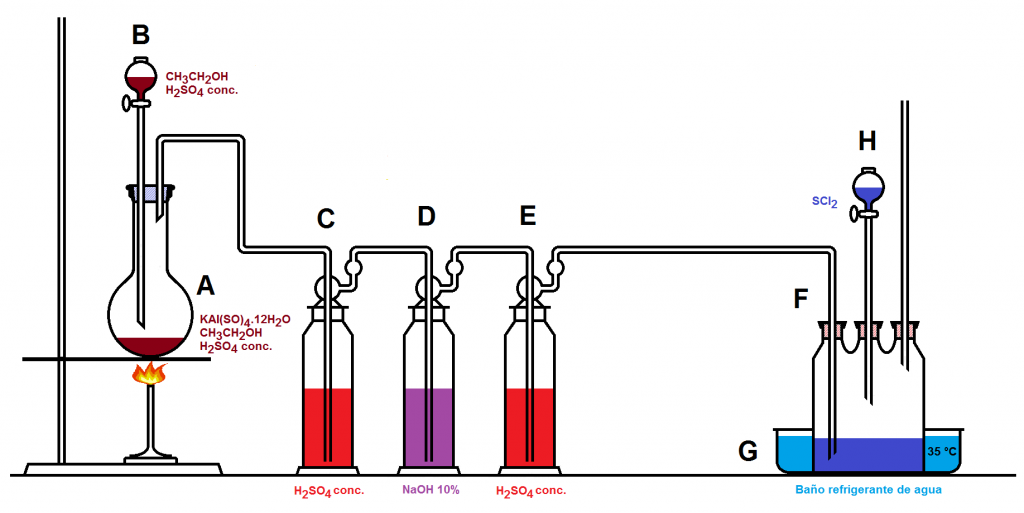
Sistema desplegable de hidrólisis (FDHS, Field Deployable Hidrolysis System)
El 11 de junio de 2015 finalizaba la destrucción del DF al concluir, en las instalaciones de Ekokem Riihimäki Waste Disposal, en Finlandia, la incineración de las 5463 tm del efluente procedente de la hidrólisis y neutralización del DF11.
Referencias
- «The Preparatory Manual of Chemical Warfare Agents», Jared B. Ledgard,The Paranoid Publications Group, 2003
- «La destrucción de las armas químicas sirias: la guerra de los números y las letras», Juan Domingo y René Pita, Documento de Opinión del Instituto Español de Estudios Estratégicos 8/2014, 16 de enero de 2014.
- «Not so deadlines», Jean Pascal Zanders, The Trench, 24 de noviembre de 2013, disponible en http://www.the-trench.org/not-so-dead-lines/; y «Not so deadlines, – some updates and correction», Jean Pascal Zanders, The Trench, 6 de diciembre de 2013, disponible en http://www.the-trench.org/not-so-dead-lines-%e2%80%92-some-updates-and-corrections/.
- «U.S. Completes Destruction of Sarin Precursors from Syria on the Cape Ray», OPCW, https://www.opcw.org/news/article/us-completes-destruction-of-sarin-precursors-from-syria-on-the-cape-ray/
- «DF Effluent Characterization Summary», https://www.google.es/url?sa=t&rct=j&q=&esrc=s&source=web&cd=1&ved=0ahUKEwj5yYP8s_LTAhWEXhoKHaoBAxEQFggnMAA&url=https%3A%2F%2Fwww.ungm.org%2FUNUser%2FDocuments%2FDownloadPublicDocument%3FdocId%3D242857&usg=AFQjCNFljXnQ_I0AN4W2T6lB-Z3nC9uzHw&sig2=9MipH-4D-gTm–lff1jmlA
- «Handbook Of Chemical And Biological Warfare Agents», Hank Ellison
- «Potential military chemical-biological agents and compounds», FM 3-11.9, MCRP 3-37.1B, NTRP 3-11.32, AFTTP(I) 3-2.55, January 2005
- «Best Synthetic Methods-Organophosphorus (V) Chemistry», «Chapter 2. Phosphonyl Compounds», Christopher M. Timperley, Academic Press, 2015
- «Convención sobre la prohibición del desarrollo, la producción, el almacenamiento y el empleo de armas químicas y sobre su destrucción», texto completo, https://www.opcw.org/sp/convencion-sobre-las-armas-quimicas/texto-completo/
- «The Field Deployable Hydrolysis System (FDHS)», Edgewood Chemical Biological Center (ECBC), https://www.ecbc.army.mil/cbarr/newsletter/2013/CBARR_August2013.pdf)
- «Disposal of effluents from neutralised Syrian chemical weapons completed», https://www.opcw.org/news/article/disposal-of-effluents-from-neutralised-syrian-chemical-weapons-completed/