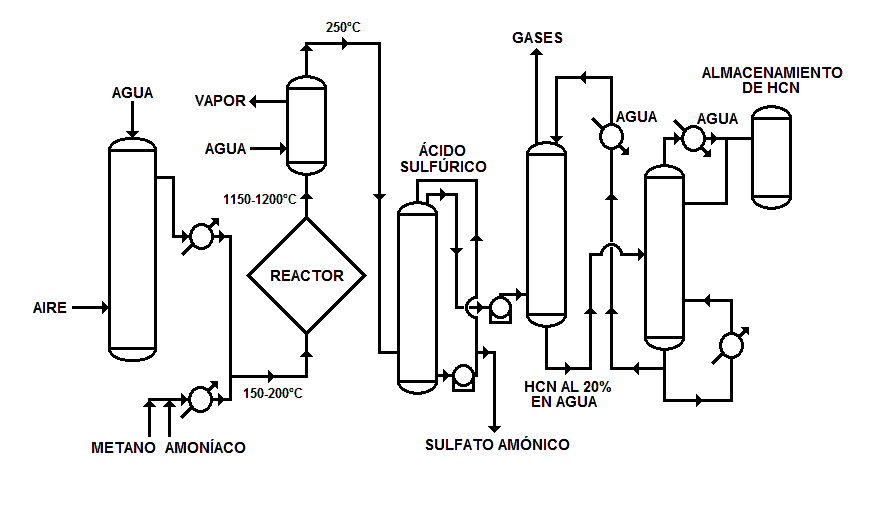
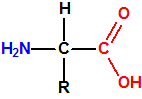
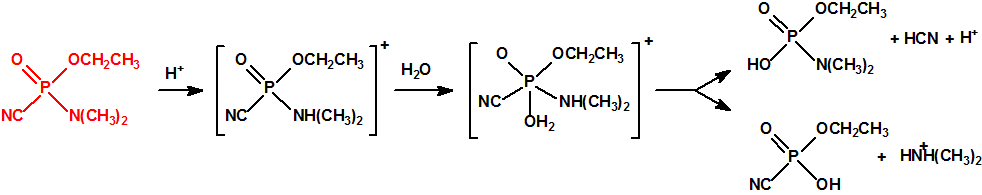
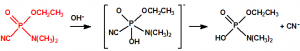
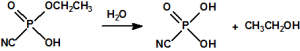
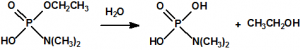
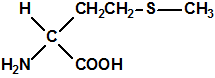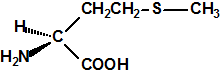Mañana, 29 de abril de 2017 se cumplirán 20 años desde que entró en vigor la Convención sobre la Prohibición del Desarrollo, la Producción, el Almacenamiento y el Empleo de Armas Químicas y sobre su Destrucción (de manera abreviada, Convención sobre la prohibición de las Armas Químicas, o CAQ). La CAQ es un tratado de no-proliferación y desarme, que, como recoge en su artículo I, prohíbe el desarrollo, la producción, la transferencia, el almacenamiento y el empleo de armas químicas, y además obliga a los Estados Partes poseedores de armas químicas e instalaciones de armas químicas, a su destrucción (en el caso de las instalaciones es posible su conversión para fines no prohibidos). El acontecimiento significó la culminación de muchos años de laboriosas negociaciones primero en la Conferencia de Desarme, y luego en la Comisión Preparatoria, y el nacimiento de un sistema internacional de desarme y verificación bajo la supervisión de la Organización para la Prohibición de las Armas Químicas (OPAQ). La CAQ, en bien de toda la humanidad, intenta excluir completamente la posibilidad de empleo de armas químicas.1
Las armas químicas antes de la 1ª Guerra Mundial1
Las sustancias químicas tóxicas han sido empleadas de manera rudimentaria como armas desde hace miles de años, por ejemplo, en forma de flechas envenenadas o de humos tóxicos, pero su empleo ha estado siempre mal visto por estar asociadas a una crueldad innecesaria y a la idea de «juego sucio», elementos ambos contrarios a las reglas de las contiendas bélicas «civilizadas». Por ello, desde muy temprano hubo algunos intentos por prohibir las armas químicas a través de diferentes tratados con escaso éxito.
El primer acuerdo internacional para limitar el empleo de armas químicas data de año 1675, cuando Francia y Alemania convinieron formalmente, en Estrasburgo, prohibir el empleo de balas envenenadas.
Casi 200 años después, en 1874 y en esa misma línea, se acordó en Bruselas el Proyecto de declaración internacional relativa a las leyes y costumbres de la guerra. El acuerdo de Bruselas prohibía el empleo de venenos o armas envenenadas y de armas, proyectiles o materiales que causaran un sufrimiento innecesario, pero el acuerdo nunca llegó a entrar en vigor.
Antes de finalizar el siglo XIX hubo un tercer acuerdo, en la Conferencia de la Haya l Protocolo de la Haya, donde las partes contratantes se prohibieron «el empleo de proyectiles cuyo único objeto sea la diseminación de gases asfixiantes o nocivos». En el año 1907, una segunda Convención de La Haya reiteró las prohibiciones anteriores de empleo de venenos o de armas envenenadas.
El nacimiento de la guerra química y las dos Guerras Mundiales
La guerra química entendida como tal comenzó el 22 de abril de 1.915, a las 5 de la mañana, cuando desde las trincheras alemanas se liberaron el frente de Ypres, a lo largo de una línea de 6 kilómetros, unas 168 toneladas de cloro procedentes de unas 5700 bombonas. La nube amarillo-verdosa de cloro, más densa que el aire y transportada por un viento favorable, sembró la muerte en las líneas anglofrancesas. Un par de años después en plena guerra química, en la noche del 11 de julio de 1917, los alemanes bombardean a las tropas inglesas de Ypres con proyectiles químicos marcados con una cruz amarilla y cargados con un nuevo agresivo, de fuerte olor a mostaza. Este agresivo vesicante produjo más de 6000 bajas y pasó a conocerse como gas mostaza o iperita. Al terminar la guerra se habían liberado entre ambos bandos más de 124200 toneladas de cloro, iperita o gas mostaza y otros agentes químicos, y se estima que más de 90000 soldados habrían sufrido la muerte a causa de estos agentes químicos.
Tras la primera guerra mundial, el 17 de junio de 1925 se produjo la firma del Protocolo de Ginebra, que expresaba la condena internacional del empleo durante los conflictos de los gases asfixiantes, tóxicos o similares y de medios bacteriológicos. Sin embargo este Protocolo no prohíbe el desarrollo, producción o posesión de armas químicas, tan sólo prohíbe el empleo de armas químicas y bacteriológicas (biológicas) con fines bélicos. Además, muchos de los países ratificaron el Protocolo reservándose el derecho de emplear armas químicas frente a países que no se habían adherido a él, o de responder por los mismos medios en caso de ser atacados con tales armas. Tras la entrada en vigor del Protocolo de Ginebra, el 8 de febrero de 1928, algunos de esos Estados Partes retiraron sus reservas y aceptaron la prohibición absoluta del empleo de armas químicas y biológicas.
Antes de que empezase la Segunda Guerra Mundial se descubrieron de manera accidental los agentes neurotóxicos (la serie G) y también las mostazas de nitrógeno (agentes vesicantes), y finalizada la contienda, sin que hubiese empleo de agentes químicos de guerra, se descubrieron otros nuevos agentes químicos como los agentes neurotóxicos de la serie V y los agentes incapacitantes (representados por el agente BZ).
La guerra Irán-Iraq y el Grupo Australia2,3,4
La guerra Irán-Iraq (1980-1988) surgió como consecuencia de diversos factores, que van más allá de la simple rivalidad entre árabes y persas: las fuertes tensiones religiosas entre chiitas (Irán) y suníes (Iraq), y la disputa por los territorios de la región de Shatt al-Arab, confluencia de los ríos Éufrates y Tigris en la ciudad de Al-Qurna, en la provincia de Basora.
A pesar de que tanto Iraq como Irán habían ratificado el Protocolo de Ginebra en 1929 y 1931, respectivamente (Iraq con la reserva de «no primer uso»), el curso de la guerra que presagiaba ser larga y difícil, llevó por parte de Iraq al empleo de armas químicas a gran escala contra los iraníes y los refugiados kurdos, a partir de 1984, En marzo de 1988 tuvo lugar el famoso ataque químico a Halabja, localidad kurdo-iraquí situada en el noreste de Iraq, cerca de la frontera con Irán. Todo apunta a que los iraquíes emplearon en los años 1983-1988 bombas químicas de 250 kg y 500 kg, proyectiles y cohetes, cargados sobre todo con iperita, sarín y tabún, y que ello fue posible porque numerosas naciones occidentales, entre las que cabe destacar Estados Unidos y Alemania, habían proporcionado a Iraq la tecnología y los precursores químicos necesarios.
En abril de 1984, como respuesta a las averiguaciones realizadas por una misión especial de investigación enviada por el Secretario General de las Naciones Unidas a Irán, que concluía que se habían empleado armas químicas en la guerra Irán-Iraq, varios gobiernos adoptaron medidas para regular la exportación de diversas sustancias químicas utilizadas para la fabricación de armas químicas. En junio de 1985 quince países acordaron coordinar sus exportaciones y se reunieron por primera vez en la embajada de Australia en Bruselas, de ahí el nombre de Grupo Australia; en la actualidad el Grupo cuenta con 42 miembros que se reúnen una vez al año en París. Todos los miembros del Grupo Australia son Estados Parte en la Convención de Armas Químicas (CAQ) y en la Convención de Armas Biológicas (CAB), y apoyan los esfuerzos realizados en el marco de ambas Convenciones para librar al mundo de las armas químicas y biológicas.
En un principio existían diferentes opiniones sobre qué precursores químicos deberían ser objeto de control de exportaciones, pero actualmente, los miembros del grupo mantienen controles de exportación sobre una lista de 64 sustancias químicas, 25 de las cuales no están recogidas en las Listas de la Convención sobre Armas Químicas.
La Conferencia de Desarme y la Comisión Preparatoria5,6,7
Durante buena parte de la última posguerra, y eclipsadas por la preocupación que suscitaba una posible guerra nuclear, las armas químicas no suscitaron gran interés hasta 1968, en que se emprendieron conversaciones sobre las armas químicas y biológicas en la Conferencia de desarme de Ginebra. Los tratados en que desembocaron aquellas conversaciones siguieron caminos divergentes.
La Convención sobre las Armas Biológicas (CAB), redactada en un breve espacio de tiempo y carente de medidas de verificación, quedó dispuesta para su firma el 10 de abril de 1972, y entró en vigor el 26 de marzo de 1975 cuando veintidós gobiernos depositaron su instrumento de ratificación.
Las negociaciones sobre la CAQ duraron mucho más, y en 1980, la Conferencia de Desarme estableció un grupo de trabajo específico sobre las armas químicas. Cuatro años después, se encomendó al grupo elaborar los términos de una eventual prohibición de las armas químicas, y de ese encargo surgió un texto de propuestas sobre la Convención. La mejora de las relaciones entre las grandes potencias a finales de los años 80, el ataque químico de 1988 contra Halabja, en Iraq, la publicidad que se dio a la amenaza de guerra química durante la guerra del Golfo y el anuncio de un acuerdo bilateral entre los Estados Unidos y la Unión Soviética para destruir la mayor parte de sus existencias de armas químicas y detener su producción impulsaron las negociaciones.
Finalmente, tras doce años de negociaciones, el 3 de septiembre de 1992, se adoptó en la Conferencia de Desarme en Ginebra el texto de la Convención sobre Armas Químicas. La CAQ se abrió a la firma el 13 de enero de 1993 en París y conforme indicaba su artículo XXI la CAQ entraría en vigor «180 días después de la fecha del depósito del sexagésimo quinto instrumento de ratificación, pero, en ningún caso, antes de transcurridos dos años del momento en que hubiera quedado abierta a la firma».
Con el fin de prepararse para la entrada en vigor del texto de la Convención, se creó una Comisión Preparatoria de la Organización para la Prohibición de las Armas Químicas, encargada de preparar procedimientos operativos detallados, así como de disponer la infraestructura necesaria para el organismo de ejecución permanente, según lo establece la Convención. La sede de la OPAQ se estableció en La Haya, Holanda. «. El 31 de octubre de 1996, Hungría entregaba su instrumento de ratificación y se convertía en el sexagésimo quinto Estado Parte, con lo cual la CAQ entraría en vigor 180 días más tarde, el 29 de abril de 1997.
La OPAQ y su Consejo Ejecutivo
Conforme estipula el Artículo VIII de la CAQ, La Organización para la Prohibición de la Armas Químicas está integrada por tres grandes órganos5:
- la Conferencia de los Estados Partes (Artículo VIII, Apartado B, artículos 9-22)
- el Consejo Ejecutivo (Artículo VIII, Apartado C, artículos 23-36), y
- la Secretaría Técnica (Artículo VIII, Apartado D, artículos 37-47)
El Consejo Ejecutivo es el órgano de gobierno de la OPAQ, responsable ante la Conferencia de Estados Partes. Está constituido de manera similar a la Junta de Gobernadores del Organismo Internacional de Energía Atómica (OIEA) y ninguno de sus miembros tiene derecho de veto, cosa que si sucede en el Consejo de Seguridad de la ONU, donde los Estados Unidos, el Reino Unido, la República Francesa, la Federación Rusa y la República Popular China tienen derecho de veto.7
El Consejo Ejecutivo es el órgano ejecutivo de la OPAQ, integrado por 41 miembros elegidos por la Conferencia por un mandato de dos años. Para garantizar el eficaz funcionamiento del Consejo, la CAQ exige que en cuanto a su composición se tome especialmente en consideración la necesidad de garantizar una distribución geográfica equitativa, la importancia de la industria química y los intereses políticos y de seguridad.8
El mandato del Consejo consiste en promover la eficaz aplicación y cumplimiento de la Convención, así como supervisar las actividades de la Secretaría Técnica, colaborar con la Autoridad Nacional de cada Estado Parte y facilitar las consultas y la colaboración entre los Estados Partes a petición de éstos.9
Cada Estado Parte tiene el derecho, de conformidad con el principio de rotación, a formar parte del Consejo Ejecutivo. Cada grupo regional está representado en el Consejo de conformidad con una fórmula detallada que se estipula en la Convención, como sigue:
- África, nueve miembros;
- Asia, nueve miembros;
- Europa Oriental, cinco miembros;
- América Latina y el Caribe, siete miembros;
- Europa occidental y otros Estados, diez miembros;
- y otro Estado Parte, designado consecutivamente, de las regiones de América Latina y el Caribe y Asia.
Actualmente, desde el 12 de mayo de 2016 al 12 de mayo de 2017, el Consejo Ejecutivo tiene la siguiente composición:
- África: Argelia (2018), Camerún (2017), Ghana (2018), Kenia (2017), Libia (2018), Marruecos (2017), Senegal (2017), Sudáfrica (2018), y Sudan (2017).
- Asia: Bangladesh (2018), China (2017), India (2017), Irán (2018), Iraq (2017), Japón (2017), Paquistán (2018), República of Corea (2017), Arabia Saudí (2017), y Vietnam (2018).
- Europa Oriental: Armenia (2017), Letonia (2017), Polonia (2018), Rusia (2018), and Eslovaquia (2018).
- América Latina y el Caribe: Argentina (2017), Brasil (2017), Chile (2018), Guatemala (2018), Méjico (2017), Panamá (2018) y Perú (2018).
- Europa occidental y otros Estados: Australia (2018), Bélgica (2018), Francia (2017), Alemania (2017), Italia (2017), España (2018), Suecia (2018), Suiza (2018), Reino Unido de Gran Bretaña e Irlanda del Norte (2017) y Estados Unidos de América (2017).
El Consejo Ejecutivo desempeña los poderes y funciones que le atribuye la Convención, así como las funciones que le delegue la Conferencia. Cumple esas funciones de conformidad con las recomendaciones, decisiones y directrices de la Conferencia y asegura su constante y adecuada aplicación. Entre las funciones más destacadas del Consejo se cuentan las siguientes:
- tomar medidas en caso de incumplimiento por un Estado Parte, incluida la presentación de recomendaciones para la acción de la Conferencia;
- estudiar y presentar a la Conferencia el proyecto de programa y presupuesto de la OPAQ;
- realizar el proyecto de informe de la Organización sobre el estado de aplicación de la Convención y el informe del Consejo sobre el desempeño de sus actividades;
- y efectuar una recomendación respecto del nombramiento del Director General.
El Consejo ejerce una función esencial en la resolución de ambigüedades y preocupaciones en materia de cumplimiento. Como ya se ha descrito, y como se comenta en mayor detalle en las secciones correspondientes a las inspecciones por denuncia y las investigaciones en casos de presunto empleo, el Consejo es el punto de contacto principal designado por la Convención para la resolución de estos asuntos.
El Consejo también tiene asignada una función especial respecto de las solicitudes de asistencia y protección contra el empleo o la amenaza de empleo de armas químicas, en virtud del Artículo X de la Convención. En el Consejo Ejecutivo no hay Estados Parte con derecho a veto.
El Consejo celebra períodos ordinarios de sesiones y reuniones. Ha venido siendo habitual que el Consejo celebre entre cuatro y seis períodos ordinarios de sesiones al año. Entre períodos ordinarios de sesiones, también puede celebrar reuniones extraordinarias con la frecuencia que pueda ser necesaria para el ejercicio de sus poderes y funciones.
De conformidad con su Reglamento el Consejo Ejecutivo adoptará las decisiones sobre temas de fondo por una mayoría de dos tercios, y las decisiones sobre cuestiones de procedimiento por mayoría simple de sus miembros. La única salvedad se corresponde a la decisión del Consejo Ejecutivo en contra de realizar una inspección por denuncia. Esta decisión solamente se podrá adoptar por una mayoría de las tres cuartas partes de todos los miembros del Consejo Ejecutivo.
El premio Nobel de la Paz
El 11 de octubre de 2013 el Comité Nobel noruego decidía otorgar el Premio Nobel de la Paz para el 2013 a la Organización para la Prohibición de las Armas Químicas (OPAQ) por sus grandes esfuerzos para eliminar las armas químicas10. Por esas fechas, con el acceso de la Republica Árabe Siria a la CAQ, eran 190 los Estados Parte que la habían ratificado, y quedaban sólo Israel que la había firmado pero no ratificado y Angola, Corea del Norte, Egipto, Myanmar (Birmania), y Sudán del sur11,12,13. El 7 de agosto de 2015 la CAQ entraba en vigor para Myanmar14, que se constituía en el Estado Parte 191, y el 16 de octubre de 2015, se rompía el capicúa, cuando la CAQ entraba en vigor para Angola15, que se constituía en el Estado Parte 192.
El comunicado noruego también resaltaba que los plazos establecidos para la destrucción de las armas químicas tampoco se habían respetado, y mencionaba expresamente a Estados Unidos y a Rusia.
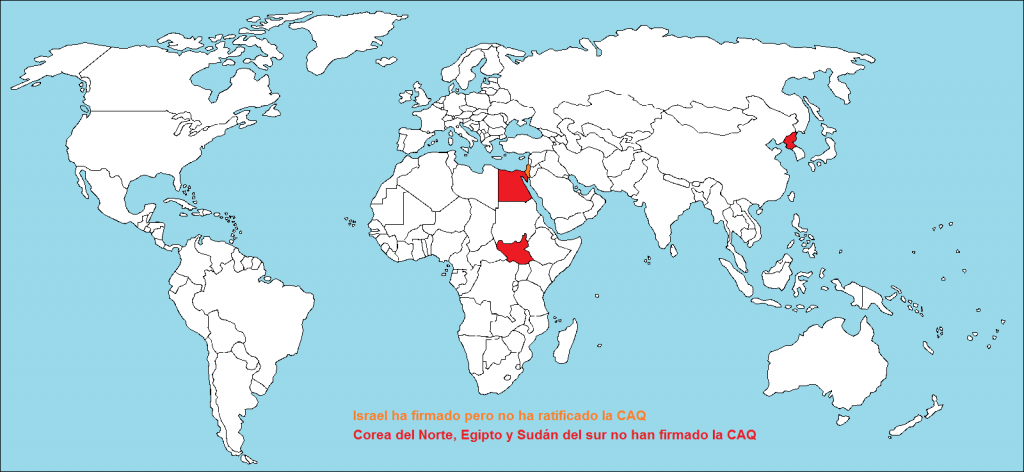 A fecha 29 de abril de 2017 tan solo 4 Estados no han ratificado la CAQ
A fecha 29 de abril de 2017 tan solo 4 Estados no han ratificado la CAQ
La CAQ se tambalea
La OPAQ justo antes de recibir el premio Nobel de la Paz sufrió una importante sacudida, que no sería la última, con motivo de la adhesión de Siria a la CAQ y la destrucción de sus armas químicas fuera de su territorio.
Recordemos que el 14 de septiembre de 2013 el Secretario General de la ONU comunicaba haber recibido de Siria, conforme estipula el artículo XXIII de la CAQ, su solicitud de adhesión a la Convención de Armas Químicas (CAQ) y que también ese día, EE.UU. y Rusia hacían público un acuerdo para destruir el arsenal químico sirio y evitar así una acción de castigo solicitada insistentemente tras los incidentes de Ghouta, el 21 de agosto de 2013. En este acuerdo, EE.UU. y Rusia se comprometían a preparar y remitir al Consejo Ejecutivo de la OPAQ un borrador con «procedimientos especiales» para la destrucción rápida del programa sirio de armas químicas y su rigurosa verificación. Este acuerdo incluía la destrucción de toda la capacidad química siria antes del 30 de junio de 201416,17.
El 15 de noviembre de 2013 el Consejo Ejecutivo de la OPAQ aprobó el plan detallado de destrucción para eliminar el arsenal sirio de armas químicas de la «manera más rápida y segura», que tenía como objetivo más importante completar la destrucción antes de la primera mitad de 2014, según lo que había establecido en la decisión del Consejo Ejecutivo de la OPAQ y en la resolución del Consejo de Seguridad de la ONU 2118 (2013), ambas de 27 de septiembre de 201316,18.
En una reunión del Consejo Ejecutivo de la OPAQ celebrada el 29 de abril de 2014 se aprobó la creación de una misión de la OPAQ para establecer los hechos que rodean a las denuncias de empleo de cloro en Siria. La Misión de Determinación de los Hechos (FFM, Fact Finding Mission) fue aceptada por el gobierno sirio, que se comprometió a proporcionar seguridad en las zonas bajo su control. El Secretario General de la Organización de las Naciones Unidas (ONU), Ban Ki-moon también expresó su apoyo, y aseguró que la ONU proporcionaría la asistencia logística y de seguridad requerida por la misión19.
Como se recordará ningún Estado Parte en la CAQ se ofreció para la destrucción en su propio territorio de las armas químicas sirias, así que finalmente se acordó su destrucción fuera de Siria. Una parte sería destruida directamente por las empresas EKOKEM (Finlandia), VEOLIA (Estados Unidos y Reino Unido) y MEXICHEM (Reino Unido), mientras que otra parte sería trasvasada al buque norteamericano MV Cape Ray para su hidrólisis en alta mar, en aguas internacionales, y luego los hidrolizados serían entregados para su destrucción a las empresas GEKA MBH (Alemania) y EKOKEM (Finlandia)16,20.
Sobrepasada la fecha incumplida del 30 de junio de 2014, el Cape Ray con la iperita y el DF en sus bodegas, abandonaba el 3 de julio de 2014 el puerto italiano de Gioia Tauro, con destino a aguas internacionales no conocidas para neutralizar por hidrólisis la iperita y el DF. Finalizada la hidrólisis, el 19 de agosto de 2014, puso rumbo al puerto finlandés de Hamina Kotka, para entregar a la empresa EKOKEM (Finlandia) 5463 toneladas de hidrolizado de DF (procedentes de 540 toneladas de DF), para su destrucción por incineración, y luego, rumbo al puerto alemán de Bremen, para entregar a la empresa GEKA MHB (Alemania) 335,5 toneladas de hidrolizado de iperita (procedentes de 20,25 toneladas de iperita), para su destrucción también por incineración16,21.
El lunes 4 de enero de 2016, la OPAQ anunciaba en su página web que se había completado la destrucción de las armas químicas sirias16,22.
Una nueva sacudida tiene lugar cuando con la República Árabe Siria siendo Estado Parte en la CAQ, la guerra continúa y continúan también las acusaciones sobre el presunto empleo de armas químicas por parte del gobierno sirio. Ningún Estado Parte solicita, conforme establece la CAQ, una solicitud para una inspección por presunto empleo, y el 7 de agosto de 2015, el Consejo de Seguridad de las Naciones Unidas aprueba la resolución 2235 (2015) para establecer un Mecanismo Conjunto de Investigación (JIM, Joint Investigation Mechanism) para identificar a los individuos o entidades responsables de uso de armas químicas en la guerra civil siria23.
La siguiente sacudida tiene lugar cuando Libia dice que quiere ser como Siria, y solicita que sus armas químicas pendientes de destruir sean retiradas de su territorio y destruidas fuera del mismo. De nuevo la ONU asume la responsabilidad, y mediante la Resolución 2298 (2016), aprobada por el Consejo de Seguridad en su 7743ª sesión, celebrada el 22 de julio de 2016, autoriza la retirada y destrucción ante la posibilidad de que agentes no estatales adquieran armas químicas en Libia representa una amenaza a la paz y la seguridad internacionales hace suya la decisión EC-M-52/DEC.1 del Consejo Ejecutivo de la OPAQ de 20 de julio, en la que solicita al Director General que ayude a Libia a elaborar un plan modificado de destrucción de las armas químicas de Libia24.
No terminan aquí las sacudidas, pues a las acusaciones de presunto empleo de armas química por parte de Siria se le suma el presunto empleo de armas químicas por parte del Gobierno de Sudán. El tema, de escaso interés para Occidente, se zanja básicamente con unas breves notas de prensa de la OPAQ expresando su preocupación. Algunos medios de comunicación destacan además que en vez de tomar cartas en el asunto se premia a Sudán con un puesto privilegiado como «Deputy Chairperson» en el Consejo Ejecutivo25,26,27.
Más acusaciones de empleo de armas químicas esta vez el 4 de abril de 2017, en el área de Khan Sheikhun en la provincia de Idlib en Siria. De nuevo, ningún Estado Parte solicita una inspección por presunto empleo como recoge la CAQ. Los Estados Unidos de manera unilateral deciden por todos y su presidente Donald Trump ordena el bombardeo de instalaciones militares del aeropuerto de Shairat, de donde habrían despegado los aviones sirios responsables del ataque, dejando de lado las disposiciones de la CAQ28,29,30,31,32.
En una propuesta rechazada por el Consejo Ejecutivo Rusia e Irán pedían al Director General que estableciera, de conformidad con el artículo IX de la Convención (Consultas, cooperación y determinación de los hechos), un grupo de expertos para investigar inmediatamente el incidente de presunto empleo de armas químicas en la República Árabe Siria el 4 de abril de 2017. Pedían además al Director General que asegurase que el grupo realizaría su labor de conformidad con la metodología de investigación del presunto empleo de armas químicas, con arreglo a la Parte XI del Anexo sobre la aplicación y la verificación de la Convención (Investigaciones en casos de presunto empleo de armas químicas) y señalaban que las conclusiones del grupo deberían basarse fundamentalmente en las pruebas materiales que se recabasen en esos lugares. El mandato del grupo debería consistir en realizar una investigación in situ sobre la manera en que las sustancias químicas tóxicas se esparcieron y emplearon, o no, en Jan Shaijun, y en verificar las denuncias sobre el almacenamiento de armas químicas en la base aérea de Shairat33,34.
El rechazo de la propuesta ruso-iraní se argumenta básicamente en que entre el FFM, y el JIM, ya creados, y en funcionamiento, se pueden llevar a cabo las investigaciones necesarias. Sin embargo, la CAQ tiene establecidos los procedimientos para realizar inspecciones por denuncia e inspecciones por presunto empleo, y para su aplicación tiene el Consejo Ejecutivo de la OPAQ, donde ninguno de sus miembros tiene derecho a veto35,36,37,38,39,40.
Tras muchos años de lucha para erradicar del mundo las armas químicas, la CAQ cumplirá su 20 aniversario, aturdida por los incidentes mencionados, como señala el título de este artículo, un aniversario agridulce para la Convención de Armas Químicas.
Referencias
- «Orígenes de la Convención sobre las Armas Químicas», https://www.opcw.org/fileadmin/OPCW/Fact_Sheets/Spanish/Fact_Sheet_1_Espanol_vs2.pdf
- «Armas químicas: la ciencia en manos del mal», René Pita Pita, Plaza y Valdés Editores, 2008
- «El Grupo Austalia», http://www.australiagroup.net/es/
- «Grupo de Australia», https://es.wikipedia.org/wiki/Grupo_de_Australia
- «Convención sobre la prohibición del desarrollo, la producción, el almacenamiento y el empleo de armas químicas y sobre su destrucción», texto completo, https://www.opcw.org/sp/convencion-sobre-las-armas-quimicas/texto-completo/
- «Convención sobre la prohibición del desarrollo, la producción, el almacenamiento y el empleo de armas químicas y sobre su destrucción», http://www.un.org/es/disarmament/wmd/chemical/index.shtml
- «The Organization for the Prohibition of Chemical Weapons and the IAEA: A comparative overview», A. Walter Dorn & Ann Rolya, IAEA Bulletin, 3/1993
- «El Consejo Ejecutivo», https://www.opcw.org/sp/acerca-de-la-opaq/consejo-ejecutivo/
- «Composición y Funciones del Consejo Ejecutivo», https://www.opcw.org/sp/acerca-de-la-opaq/consejo-ejecutivo/composicion-y-funciones/
- «The Nobel Peace Prize for 2013», http://www.nobelprize.org/nobel_prizes/peace/laureates/2013/press.html
- «OPCW to Review Request from Syria», https://www.opcw.org/news/article/opcw-to-review-request-from-syria/
- «OPCW Director-General Welcomes Agreement on Syrian Chemical Weapons», https://www.opcw.org/news/article/opcw-director-general-welcomes-agreement-on-syrian-chemical-weapons/
- «Syria’s Accession to the Chemical Weapons Convention Enters into Force», https://www.opcw.org/news/article/syrias-accession-to-the-chemical-weapons-convention-enters-into-force/
- «Myanmar Joins Chemical Weapons Convention», https://www.opcw.org/news/article/myanmar-joins-chemical-weapons-convention/
- «Angola Joins Chemical Weapons Convention», https://www.opcw.org/news/article/angola-joins-chemical-weapons-convention/
- «¿Completada la destrucción de las armas químicas sirias?», J.Domingo, https://cbrn.es/?p=433
- «Joint national paper by the Russian Federation and the United States of America framework for elimination of syrian chemical weapons», https://www.opcw.org/fileadmin/OPCW/EC/M-33/ecm33nat01_e_.pdf
- «Detailed requirements for the destruction of syrian chemical weapons and syrian chemical weapons production facilities», http://www.opcw.org/fileadmin/OPCW/EC/M-34/ecm34dec01_e_.pdf
- «OPCW to Undertake Fact-Finding Mission in Syria on Alleged Chlorine Gas Attacks», https://www.opcw.org/news/article/opcw-to-undertake-fact-finding-mission-in-syria-on-alleged-chlorine-gas-attacks/
- «La destrucción de las armas químicas sirias: la guerra de los números y las letras», Juan Domingo y René Pita, Documento de Opinión del Instituto Español de Estudios Estratégicos, 8/2014, 16 de enero de 2014, http://www.ieee.es/Galerias/fichero/docs_opinion/2014/DIEEEO08-2014_GuerraQuimica_NumsLetras_JDomingo-RenePita.pdf
- «Disposal of effluents from neutralised Syrian chemical weapons completed», http://www.opcw.org/news/article/disposal-of-effluents-from-neutralised-syrian-chemical-weapons-completed/
- «Destruction of Syrian chemical weapons completed», https://www.opcw.org/news/article/destruction-of-syrian-chemical-weapons-completed/
- «La situación en el Oriente Medio (Siria)», http://www.un.org/es/comun/docs/?symbol=S/RES/2235(2015)
- «La situación en Libia», http://www.un.org/es/comun/docs/?symbol=S/RES/2298(2016)
- «OPCW Examining NGO Report on Allegations of Chemical Weapons Use in Sudan», https://www.opcw.org/news/article/opcw-examining-ngo-report-on-allegations-of-chemical-weapons-use-in-sudan/
- «OPCW’s Initial Assessment of NGO Report on Allegations of Chemical Weapons Use in Sudan», https://www.opcw.org/news/article/opcws-initial-assessment-of-ngo-report-on-allegations-of-chemical-weapons-use-in-sudan/
- «Sudan: Elevation to OPCW’s governing body a slap in the face for victims of chemical attacks», https://www.amnesty.org/en/latest/news/2017/03/sudan-elevation-to-opcws-governing-body-a-slap-in-the-face-for-victims-of-chemical-attacks/
- «OPCW Press Release on Allegations of Chemical Weapons Use in Southern Idlib, Syria», https://www.opcw.org/news/article/opcw-press-release-on-allegations-of-chemical-weapons-use-in-southern-idlib-syria/
- «Worst Chemical Attack in Years in Syria; U.S. Blames Assad», https://www.nytimes.com/2017/04/04/world/middleeast/syria-gas-attack.html?_r=0
- «Un supuesto ataque químico causa una matanza en la zona rebelde siria», http://internacional.elpais.com/internacional/2017/04/04/actualidad/1491292477_793091.html
- «La condena del ataque químico en Siria enfrenta a EE.UU. y Rusia», http://www.lavanguardia.com/internacional/20170405/421466091056/comunidad-internacional-acusa-asad-ataque-quimico-grave-ultimos-anos-siria.html
- «Estados Unidos ataca con misiles al régimen sirio», http://internacional.elpais.com/internacional/2017/04/06/estados_unidos/1491506181_402836.html
- «Report of the Fifty-Fourth Meeting of the Executive Council»,https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/ecm5402_e_.pdf
- «Draft OPCW decision on Syria chemical incident that Russia proposed and UK opposed», http://rusemb.org.uk/fnapr/6064
- «Germany: Statement at the 54th Meeting of the Executive Council on 20 April 2017», https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/Germany_ECM54_20-04-2017.pdf
- «France: Statement at the 54th Meeting of the Executive Council», https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/France_ECM-54.pdf
- «United Kingdom: Statement at the 54th Meeting of the Executive Council», https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/United_Kingdom_ECM-54.pdf
- «United States of America: Statement at the 54th Meeting of the Executive Counci», https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/United_States_ECM54_Statement.pdf
- «Islamic Republic of Iran: Statement at the 54th Meeting of the Executive Council», https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/Iran_ECM-54.pdf
- «Cuba: Statement at the 54th Meeting of the Executive Council», https://www.opcw.org/fileadmin/OPCW/EC/M-54/en/Cuba_ECM54.pdf