Como ya sabemos detección e identificación no son sinónimos1.
Hablando de detección de agentes biológicos, detección sería «la acción y efecto de poner de manifiesto por métodos físicos o químicos la presencia de agentes biológicos». Necesitamos recurrir a métodos físicos o químicos porque los agentes biológicos son prácticamente invisibles, incoloros, inodoros e insípidos, y no podemos saber si los inhalamos, ingerimos o entramos en contacto con ellos. Además, la mayoría de ellos presenta un importante periodo de latencia, es decir, desde que entramos en contacto con ellos hasta que manifestamos sus efectos pueden transcurrir largos periodos de tiempo.
En una situación real los detectores biológicos y los síntomas reconocidos (éstos, transcurridos un cierto tiempo más o menos largo) pueden dar una primera indicación del posible uso y de la naturaleza del agente biológico.
Al igual que en el caso de los agentes químicos, para los agentes biológicos también podemos distinguir, en el proceso de detección, diferentes niveles de conocimiento o información, función de la información suministrada por el detector o detectores.
¿Cuántos niveles de detección hay?. Pues como el caso de los agentes químicos no hay unanimidad al respecto, algunas fuentes hablan de cuatro niveles (indicativo, presunto, definitivo y probatorio) que a veces se reducen a tres (indicativo, presunto y definitivo). Sin embargo en este documento se propone, igual que se ha venido haciendo desde hace muchos años para los agentes químicos2,3,4, el establecimiento de tan solo dos niveles. Estos dos niveles de detección serían:
- detección provisional
- detección confirmada
La detección provisional es la obtenida mediante la respuesta de un detector en combinación o no con la información sobre sus efectos.
La detección confirmada es la conseguida mediante el empleo de dos detectores con tecnologías diferentes para de este modo minimizar los posibles falsos positivos.
Si se desea saber más acerca del agente biológico hay que recurrir a la identificación biológica, para la cual, al igual que en la identificación de los agentes químicos y de las toxinas, se distinguen tres niveles en función de la información obtenida6:
- identificación provisional
- identificación confirmada
- identificación inequívoca
Detección biológica
El objetivo de un sistema de detección biológica es simplemente poner de manifiesto (detectar) la presencia de material biológico en una muestra5. Por lo general, las tecnologías empleadas por los detectores biológicos buscan la presencia de proteínas, ácido desoxirribonucleico (ADN), ácido ribonucleico (ARN) o trifosfato de adenosina (ATP).
Las proteínas y el ADN se encuentran en todas las células, incluyendo células epiteliales, esporas y células bacterianas, mientras que el ATP es un metabolito presente sólo en las células vivas. Las toxinas biológicas (por ejemplo, ricina y toxina botulínica) están basadas en proteínas, pero las muestras de toxinas también pueden contener ADN si el material se prepara en crudo a partir de las células que producen la toxina. Por ejemplo, la presencia de toxinas botulínicas o de la ricina está indicada por la presencia del ADN de Clostridium botulinum y del Ricinus communis, respectivamente.
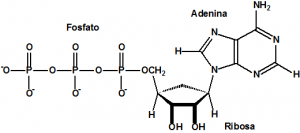
Molécula de trifosfato de adenosina (ATP)
Además de los ensayos indicadores de la presencia de proteínas, ADN/ARN y ATP, también se puede utilizar la espectroscopia FTIR para establecer la posible presencia o ausencia de materiales biológicos en una muestra. La espectroscopia FTIR es una técnica relativamente simple, utilizada por los primeros intervinientes en un incidente químico, que proporciona información sobre la naturaleza de la muestra comparando el espectro de la muestra en una librería que contiene los espectros de miles de compuestos.
Normalmente, si el espectro de la muestra no está en la librería, el algoritmo del software del equipo intentará clasificarlo en función de sus características espectrales (presencia o ausencia de distintas bandas o picos). Algunos espectrómetros FTIR disponen de algoritmos de análisis espectral para indicar si una muestra puede contener o no material biológico en base a la presencia de proteínas, ácidos grasos, fosfolípidos o/y carbohidratos.
A pesar de que los ensayos indicadores de material biológico son relativamente rápidos y baratos, se deben utilizar con precaución, y si es posible conjuntamente con otros sistemas más específicos. Los ensayos indicadores de material biológico tienen en general baja especificidad (es decir, pueden provocar falsos positivos) y baja sensibilidad (es decir, puede provocar falsos negativos). Los ensayos indicadores de material biológico detectan una amplia gama de materiales orgánicos y biológicos, pero no aseguran la presencia de agentes biológicos específicos.
Tenemos diferentes tipos de ensayos más o menos rápidos y específicos:
- Ensayo de proteína
- Ensayo de ADN
- Ensayo de ATP
- Espectroscopía FTIR
Ensayo de proteína
Los ensayos de proteína5 detectan cualquier tipo de proteína (incluidas las proteínas de la leche en la crema de café y en la leche en polvo) y pueden incluso acompañarse de un ensayo de pH (el material biológico presenta por lo general un pH neutro) o/y de un ensayo de almidón (indicativo de un ingrediente alimentario).
Son fáciles de utilizar (añadir o tomar la muestra con un hisopo, mezclar y leer; o simplemente tomar la muestra con un hisopo y leer), y el usuario visualiza manualmente el cambio de color debido al pH, las proteínas o el almidón.
El tiempo de análisis del orden de 5 minutos o menos, con un límite de detección (LOD) que se encuentra entre 10-100 millones de esporas de Bacillus anthracis (equivalentes a unas 1000-10000 dosis infecciosas, que corresponde a una cantidad apenas visible de polvo, <1 mg).
Son ejemplos de estos sistemas el BioCheck® (20/20 Gene Systems), el INDIPRO (Macherey-Nagel) y el TASKit BioScreener™ (Field Forensics), entre otros.
Ensayo de ADN
Los ensayos de ADN5 detectan cualquier tipo de ADN (ya sea humano, animal o vegetal) y algunos tipos de ARN.
Son fáciles de utilizar (añadir la muestra, mezclar y leer), pero requieren un lector de fluorescencia.
El tiempo de análisis es del orden de 5 minutos, con un límite de detección (LOD) que se encuentra entre 1-10 billones de esporas de Bacillus anthracis (equivalentes a alrededor de 1-10 millones de dosis infecciosas, y una cantidad fácilmente visible de polvo, aproximadamente entre 1-10 mg).
El fluorómetro o fluorímetro es un equipo que requiere ciertas atenciones y es relativamente costoso (del orden de unos 10000 euros), y además el coste de los ensayos de ADN es mayor que el de los ensayos de proteína.
Un ejemplo de este tipo de sistemas es el Prime Alert® (GenPrime®)
Ensayo de ATP
Los ensayos de ATP5 comprueban si está presente y vivo algún tipo de material celular.
Son moderadamente fáciles de utilizar (el procedimiento conlleva varios etapas que incluyen entre otras pipetear y filtrar). Además, para las esporas debe realizarse antes de la detección un paso previo adicional (de aproximadamente unos 15 minutos) para estimular que las esporas pasen al estado vegetativo (celular vivo), y así permitir la detección. También se requiere de un lector óptico cuyo coste es del orden de 3000-5000 euros.
El tiempo de análisis es del orden de unos 20 minutos, con un límite de detección (LOD) que se encuentra alrededor de las 10000 esporas de Bacillus anthracis (aproximadamente una dosis infecciosa; cantidad no visible por el ojo).
Son ejemplos de estos sistemas el PROFILE® 1 (New Horizons Diagnostics) y el Clean-Trace™ (3M), entre otros.
Espectroscopia FTIR
La espectroscopia FTIR5 (Fourier Transform InfraRed spectroscopy) se utiliza principalmente para identificar fácil y rápidamente la composición química de una muestra desconocida, orgánica o inorgánica, y en estado sólido, líquido e incluso gaseoso.
Las proteínas (contenidas en muchos materiales biológicos) dan un espectro infrarrojo característico y podrían detectarse en una muestra si el contenido de proteínas en la misma es al menos de un 10%. No obstante hay que indicar que no se han realizado muchos estudios para comprobar la presencia (detección) de material biológico (por ejemplo, esporas de Bacillus anthracis) en polvos sospechosos.
La detección de material biológico se basa en la presencia en el espectro infrarrojo de la muestra sospechosa, de bandas de absorción correspondientes a proteínas, ácidos grasos, fosfolípidos o/y carbohidratos. Para la identificación de los componentes de una muestra el equipo utiliza algoritmos de comparación de espectros empleando para ello una librería de espectros de componentes conocidos. La identificación de los componentes de una mezcla NO siempre es posible.
Los sistemas de campo son pequeños, compactos, de poco peso, totalmente estancos y de uso muy simple. La estanqueidad facilita enormemente la descontaminación, si ésta fuese necesaria. Se operan con bastante facilidad mediante un teclado táctil o mediante unos simples botones.
El tiempo de análisis es del orden de unos 5 minutos, con un límite de detección (LOD) del orden del un 10 % en peso de proteína en la muestra (no se han realizados estudios detallados para determinar la sensibilidad en términos de número de esporas de Bacillus anthracis).
El coste del equipo y de las librerías es algo elevado, por encima de los 50000 euros, pero no se requieren consumibles especiales, y por tanto el coste por ensayo es prácticamente nulo.
Son ejemplos de estos sistemas, entre otros, el HazMatID Ranger™, el HazMatID™ 360, y el HazMatID™ Elite (todos ellos de Smiths Detection) y el TruDefender™ FT/FTi, el TruDefender™ FTX/FTXi y el Analizador Gemini™ (todos ellos de Thermo Scientific).
Identificación biológica
Los criterios para la identificación de los agentes biológicos de guerra recogidos por OTAN vienen descritos en el documento canadiense sobre «Preparación de muestras e identificación de agentes biológicos, químicos y de espectro medio»(Sample Preparation and Identification of Biological, Chemical and Mid-Spectrum Agents)6. Cada uno de los tres niveles de identificación (provisional, confirmada e inequívoca) está perfectamente definido, tanto para los agentes químicos y agentes de espectro medio, como para los agentes biológicos.
Identificación provisional
Se considera que un agente biológico ha sido identificado de manera provisional cuando se cumple uno de los siguientes criterios:
- La presencia de un antígeno único para el agente biológico en cuestión se pone de manifiesto por una reacción positiva con un anticuerpo específico en una prueba de inmunoensayo; o
- La presencia de una secuencia única de ácido nucleico para el agente biológico en cuestión se pone de manifiesto por una reacción positiva con una sonda específica de ácido nucleico (sonda genética) en un ensayo de PCR (Polymerase Chain Reaction, Reacción en Cadena de la Polimerasa); o
- Se obtiene una respuesta positiva por cultivo in vitro o por múltiples ensayos metabólicos
Identificación confirmada
Se considera que se ha conseguido la identificación confirmada de un agente biológico cuando se cumplen cualesquiera dos de los criterios descritos para la identificación provisional en presencia de patrones auténticos de referencia (controles positivos y negativos) en condiciones experimentales idénticas.
En el caso de los agentes biológicos, con los equipos portátiles sólo podría obtenerse una identificación provisional pues la identificación confirmada requeriría la utilización del agente biológico a identificar. La identificación confirmada podría llevarse a cabo en un laboratorio analítico desplegable NBQ, pero la identificación inequívoca probablemente pasaría por una adecuada toma de muestras, con una estricta cadena de custodia y un análisis completo en un Laboratorio de Referencia7.
Identificación inequívoca
La identificación inequívoca de un agente biológico proporciona el más alto nivel de certeza requerido para el desarrollo de posiciones estratégicas y políticas. La identificación confirmada se convierte en identificación inequívoca si se satisfacen todos los siguientes criterios para el agente biológico en cuestión en presencia de patrones auténticos de referencia (controles positivos y negativos) en condiciones experimentales idénticas:
- Se obtienen una respuesta positiva por un método de identificación genética; y
- Se obtiene una respuesta positiva por un método inmunológico; y
- Se obtiene una respuesta positiva por cultivo in vitro o por múltiples ensayos metabólico; y
- Las características de la enfermedad del agente microbiano se confirman en un modelo animal aceptado, si ese modelo existe.
Estos criterios se aplicarán a todos los microbios clásicos, con la excepción de la identificación inequívoca para:
- los agentes biológicos para los cuales no hay métodos de cultivo apropiados, por ejemplo, el virus de la hepatitis B no se puede cultivar en medios de cultivo celulares artificiales;
- los agentes biológicos que han sido manipulados genéticamente para cambiar sus características; y
- los nuevos agentes, por ejemplo, organismos microencapsulados, priones, ácidos nucleicos infecciosos, etc..
La evaluación de viabilidad del agente biológico es otro aspecto muy importante a tener en cuenta, puesto que para causar enfermedad en el anfitrión vivo los agentes biológicos deben ser metabólicamente activos y capaces de replicarse.6
Mientras no se consiga una identificación positiva mediante cultivo in vitro, ensayos metabólicos múltiples o ensayo en modelo animal, resulta imposible determinar si el agente biológico es metabólicamente activo. Mientras no se determine la existencia de actividad metabólica, existe la posibilidad de que el incidente investigado sea una falsa alarma en la cual se ha utilizado agentes biológicos muertos sólo para generar una situación de pánico.
Esta posibilidad debería ser tenida en cuenta al evaluar el tratamiento a las personas expuestas y las posibles connotaciones criminales, estratégicas y políticas de los resultados de la identificación. Esto pone de relieve la importancia de una adecuada recogida, transporte y almacenamiento de las muestras antes de su análisis, para que cualquier posible agente biológico presente en las mismas mantenga su viabilidad hasta la realización de los ensayos de identificación.
Bibliografía
- «Detección e identificación no son sinónimos», www.cbrn.es, 20 de febrero de 2015
- «To be or not to be: the need to be sure in chemical detection», Juan Domingo y René Pita, NBC International, Spring 2006, pp. 61-63
- «Detección de agentes químicos de guerra», René Pita y Juan Domingo, Revista Ejército, Año 2007, número 790, páginas 59-63.
- «What you looking at…!?», Juan Domingo y René Pita, CBRNe WORLD Summer 2009, Vol. 4, Issue 2, pp. 36-38.
- Biodetection Technologies for First Responders-2014 Edition, https://www.pnnl.gov/nationalsecurity/technical/chemical_biological/Biodetection_Technologies_for_First_Responders.pdf
- Sample Preparation and Identification of Biological, Chemical and Mid-Spectrum Agents, J.R. Hancock and D.C. Dragon, http://cradpdf.drdc-rddc.gc.ca/PDFS/unc57/p524339.pdf, o http://www.google.es/url?sa=t&rct=j&q=&esrc=s&source=web&cd=1&ved=0CCEQFjAA&url=http%3A%2F%2Fwww.dtic.mil%2Fcgi-bin%2FGetTRDoc%3FAD%3DADA443173&ei=yk3nVMTZLYOsUb-4gIAF&usg=AFQjCNFELbSn8av2rVfksg_TJZmSw5Z6Dg
- «Analyse this! «, Juan Domingo y René Pita, CBRNe WORLD , Winter 2008, pp. 38-39.