Hace no mucho tiempo alguien hacía la siguiente pregunta:
¿Conocéis alguna relación entre el ácido sulfúrico y la iperita?. ¿Algo relacionado con la síntesis de la misma?. He buscado síntesis de la HD y no veo el sulfúrico por ningún lado.
Mi respuesta fue la siguiente:
«Con respecto al ácido sulfúrico yo tengo referencia de un oficial de bomberos que lo mezclaba con sosa caústica para la obtención de la iperita. Por otro lado internet está lleno de listillos NBQ que copian a trozos y traducen una mierda. Pues sí, puedes necesitar ácido sulfúrico para una de las reacciones más tontas de síntesis orgánica, la reducción de alcoholes para obtener alquenos. En medio ácido fuerte, de ácido sulfúrico, el etanol se deshidrata produciendo etileno, pero teniendo en cuenta que el etanol es una alcohol primario y que etileno, sustancia no listada se puede obtener por otras vías, yo le daría de nota un 1, más por la escasez de ciencia que por la abundancia de imaginación.»1, 2, 3
Agentes y precursores
El anexo A sobre sustancias químicas de la Convención para la (CAQ) contiene tres listas (Lista 1, Lista 2 y Lista 3) en las que se catalogan las distintas sustancias químicas. Cada una de estas tres listas contiene una subdivisión entre sustancias químicas tóxicas (A) y precursores (B).4
La CAQ, en su Artículo II. Definiciones y Criterios, apartado 3, indica que a los efectos de la misma, se entiende por «precursor», «Cualquier reactivo químico que intervenga en cualquier fase de la producción por cualquier método de una sustancia química tóxica. Queda incluido cualquier componente clave de un sistema químico binario o de multicomponentes».4
La definición de la CAQ no es precisamente clarificadora, pero en lo referente a la producción de drogas ilícitas podemos encontrar una definición más apropiada de «precursores químicos»: «sustancias que pueden utilizarse en la producción, fabricación y/o preparación de estupefacientes, sustancias psicotrópicas o de sustancias con efectos semejantes, y que incorporan su estructura molecular al producto final, por lo que resultan fundamentales para dicho proceso».5
Una definición más corta de «precursor químico» podría ser la de «una sustancia indispensable o necesaria para producir otra diferente mediante una reacción química».6, 7
Como veremos el ácido sulfúrico no incorpora parte alguna de su estructura molecular a la estructura de la iperita y no es indispensable o necesario para la obtención de la misma, de modo que el ácido sulfúrico no es un precursor de la iperita.
El azufre de la iperita no es del ácido sulfúrico
La iperita fue descubierta por César-Mansuete Despretz8, 9 en 1822, preparada por la reacción entre el cloruro de etileno y el azufre. Después de Despretz, la iperita también fue preparada por Alfred Riche8, 10 en 1854 y más adelante Frederick Guthrie8, 11 en 1860, cuando éste último estudiaba los productos de condensación resultantes de la reacción de los compuestos halogenados de azufre con las olefinas. Más tarde, en 1896, Viktor Meyer8, 12 preparaba la iperita por cloración del tiodiglicol (Lista 2B.13, CAS 111-48-8) con tricloruro de fósforo (Lista 3B.6, CAS 7719-12-2).
También se ha preparado iperita mediante la cloración del tiodiglicol con cloruro de hidrógeno, HCl, (Hans Thacher Clarke8,13 en 1913), con cloruro de tionilo, SOCl2 (Lista 3B.14, CAS 7719-09-7), (Wilhelm Steinkopf8, 14 en 1920) y con monocloruro o dicloruro de azufre, SCl (Lista 3B.12, CAS 10025-67-9) y SCl2 (Lista 3B.13, CAS 10545-99-0), (Lundin8,15)
Mediante el método de Meyer y Stephen8, 16, puede obtenerse iperita con un rendimiento de casi el 98 %, rociando una mezcla constituida por 75 partes de SCl y 25 partes de SCI2 en una atmósfera de etileno.
Otros métodos de síntesis se basan en la foto-adición de sulfuro de hidrógeno a enlaces olefínicos8,17.
La iperita puede ser preparada fácilmente en el laboratorio siguiendo el método original de Guthrie: burbujeando etileno sobre cloruro de azufre.19
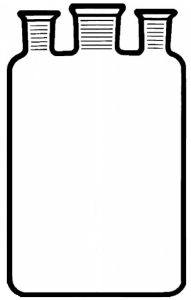
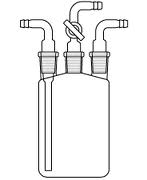
La reacción entre el etileno y el cloruro de azufre se lleva a cabo en una botella de Woulff, recipiente con tres bocas de esmerilado normalizado, normalmente sin tubuladura de fondo, de vidrio tipo 1 o vidrio neutro, esterilizable en autoclave y resistente al vacío.
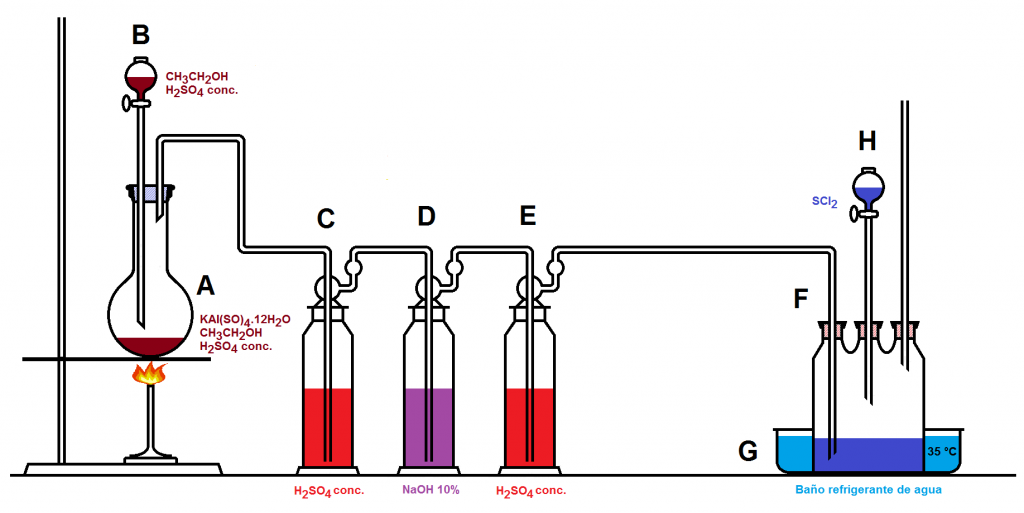
Se monta un aparato como el mostrado en la siguiente figura, donde se pueden observar tres zonas bien diferenciadas:
En la primera se genera el etileno. En un matraz de fondo redondo (A) se calienta una mezcla de alumbre, etanol y ácido sulfúrico concentrado, y se va añadiendo desde el recipiente acoplado (B) una mezcla de etanol y ácido sulfúrico concentrado para mantener la producción de etileno
En la segunda se seca el etileno. Las tres botellas de lavado (C, D, E) contienen ácido sulfúrico concentrado, hidróxido de sodio al 10% y ácido sulfúrico concentrado. No se debe conectar el sistema de secado de etileno a la botella de Woulff hasta que la producción de etileno no sea uniforme.
En la tercera se sintetiza la iperita por reacción del etileno con cloruro de azufre. En una botella de Woulff (F), sumergida en un baño refrigerante de agua (G) para que la reacción no supere los 35 °C, se hace borbotear el etileno sobre el cloruro de azufre, y se va añadiendo más cloruro de azufre desde el recipiente acoplado (H) a medida que la reacción transcurre.
Al final de la reacción la iperita se destila a presión reducida de 15 mm de Hg, recogiéndose la fracción que destila entre 106 °C y 108 °C.
Deshidratación del etanol con ácido sulfúrico19, 20, 21
El ácido sulfúrico se utiliza en este caso para la obtención del etileno por deshidratación del etanol. Esta es una práctica que habitualmente realizan los estudiantes de química orgánica, que además aprovechan el etileno para bromarlo y obtener bromuro de etileno.
La deshidratación total de alcoholes (eliminación de un mol de agua por cada mol de alcohol) es un procedimiento de laboratorio sencillo para preparación de alquenos. La deshidratación se puede efectuar calentando el alcohol en presencia de un catalizador ácido. En el laboratorio, lo más cómodo es calentar el alcohol en un matraz con un ácido protónico no volátil, como los ácidos sulfúrico o fosfórico.
La facilidad relativa de deshidratación de los distintos tipos de alcoholes disminuye en el siguiente orden: terciario > secundario > primario. Los alcoholes primarios, como el alcohol etílico, se deshidratan solamente a temperaturas elevadas, mientras que muchos alcoholes terciarios se deshidratan por la acción de los ácidos incluso a la temperatura ambiente.
Referencias
- «Takaka residents allowed to return after blaze», Errol Kiong, Wednesday Jun 22, 2005, http://www.nzherald.co.nz/nz/news/article.cfm?c_id=1&objectid=10332038
- «Chemical confusion», Rich, Wednesday, June 22, 2005, http://observationz.blogspot.com.es/2005/06/chemical-confusion.html
- «Química orgánica. Volumen 1. Principios fundamentales», I.L.Finar, 3ª edición, Editorial Alhambra, 1975, página 112.
- «Convención sobre la Prohibición del Desarrollo, la Producción, el Almacenamiento y el Empleo de Armas Químicas y sobre su Destrucción (CAQ)», disponible en https://www.opcw.org/fileadmin/OPCW/CWC/CWC_es.pdf y en https://www.opcw.org/fileadmin/OPCW/CWC/CWC_es.doc
- «Manual de sustancias químicas usadas en el procesamiento de drogas ilícitas», http://www.comunidadandina.org/Upload/20135316739manual_sustancias_quimicas.pdf
- «Precursor químico», «https://es.wikipedia.org/wiki/Precursor_qu%C3%ADmico
- «Definición de precursor», http://definicion.de/precursor/#ixzz4DwNHjGtm
- «Chemistry and Toxicology of Sulphur Mustard-A Review», R.C. Malhotra, K. Ganesan, K. Sugendran & R.V. Swamy, Defence Science Journal, vol 49, No 2, April 1999, pp. 97-116
- «Sulphur mustard preparation and properties», César-Mansuete Despretz, Annales de Chimie et de Physique, 1822, 21, 428.
- «Recherches sur des combinaisons chlorées dérivées des sulfures de méthyle et d’éthyle», M. Alfred Riche, Annales de Chimie et de Physique, 1855, 43(3), 283-304.
- «On some derivatives from olefines», F.G. Guthrie, Quart. J. Chem. Soc., 1860, 12, 116 & 1861, 13, 129-35.
- «Weitere Studien zur Kenntnis der Thiophengruppe», V. Meyer, Dtsch. Chem. Ges., 1986,19: 628–632.
- » 4-Alky-1:4-thiazans», Hans Thacher Clarke, J. Chem. Soc., 1912, 101, 1583-90.
- «Über das Thiodiglykolchlorid und einige abkömmlinge desselben», Wilhelm Steinkopf, Julius Herold & Joseph Stöhr, Chemische Berichte, 1920, 53, 1007-12.
- «Verification of dual-use chemicals under the Chemical Weapon Convention: The case of thiodiglycol», S.J. Lundin, Oxford University Press, UK, 1991.
- «Über thiodiglykolverbindungen», V. Meyer, Chemische Berichte, 1886, 19, 3259-65.
- «The photo-addition of hydrogen sulfide to olefinic bonds», W.E. Vaughn & F.F. Rust, J. Org. Chem., 1942, 7, 472-76.
- «The war gases-Chemistry and analysis», Mario Sartori, D. Van Nostrand, 1939
- «Curso práctico de química orgánica- Experiencia 12. Etileno y bromuro de etileno», R.Q. Brewster, C.A. Vanderverf & W.E. McEwen, Editorial Alhambra, 1970, pag. 62-66
- «Química orgánica-Volumen I. Principios fundamentales», I. L. Finar, 3ª edición, Editorial Alhambra, 1975, pag. 112 y 216-218
- «Química orgánica superior», L.F. Fieser & M. Fieser, Ediciones Grijalbo, vol. I, pag. 174-184